成果简介:
细菌抗生素抗性已严重威胁环境安全和公共健康,快速评估环境细菌抗生素抗性水平对遏制抗性产生和传播具有重要意义。本研究以E. coli为模式菌,构建了其在抗生素暴露下的胞内活性氧(ROS)和最小抑菌浓度(MIC)的剂量-效应关系,并据此提出了一种可快速评估抗性水平的新方法(ROS-AST)。该方法相比传统MIC测定方法(如微量肉汤稀释法等)具有快速、准确的优势。此外,E. coli在长期抗生素胁迫下的胞内ROS动态变化也可指示其抗性由可逆向不可逆转变的关键节点。该成果为环境抗生素抗性风险快速评估与动态预警提供了新方法。
全文速览:
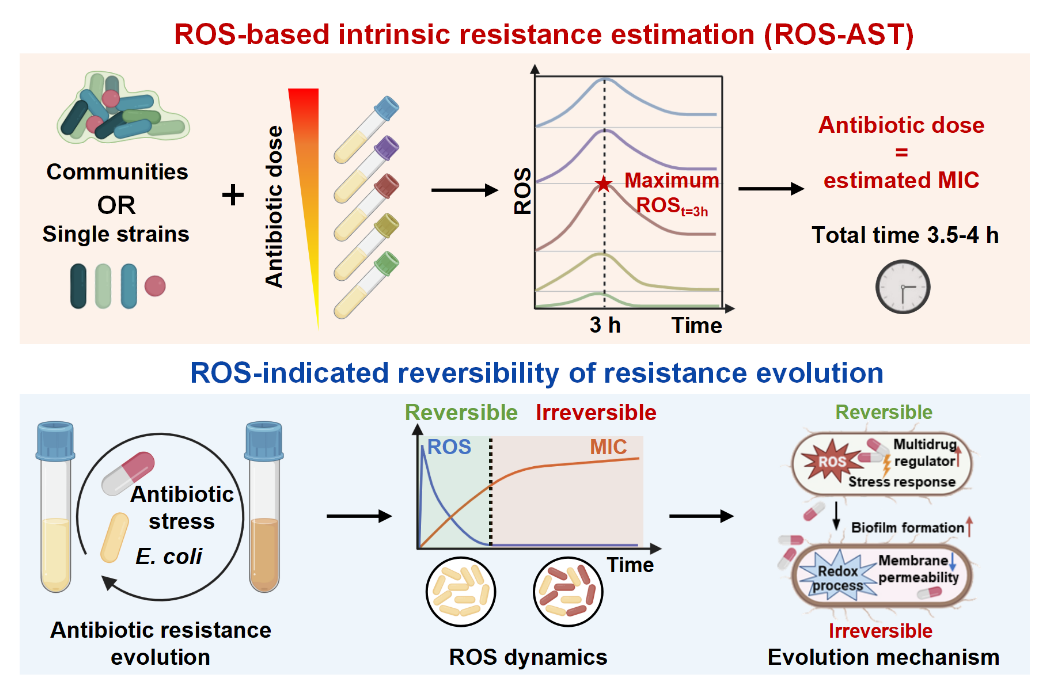
一株环境源E. coli短期暴露于梯度浓度的头孢吡肟、卡那霉素和诺氟沙星等抗生素后,胞内ROS快速积累,并在约3小时达到峰值,随后降低。该峰值浓度的最大值所对应的抗生素胁迫浓度与细菌对该抗生素的MIC相当,此为ROS-AST的工作原理。ROS-AST能在4小时内快速测定MIC并评估抗生素抗性风险,显著快于传统微量肉汤稀释法(约16小时)。经3类抗生素和26种环境细菌的验证(MIC范围为0.03-128 µg/mL),该方法准确性较高,与传统方法的平均误差仅为7.23%。ROS-AST也可对环境微生物群落(废水、土壤和地表水等)的抗生素抗性水平进行半定量评估,结果与经典圆片扩散法基本一致。
将E. coli长期暴露于亚抑制浓度卡那霉素18天,胞内ROS在前6天显著积累,在该阶段撤去抗生素胁迫,种群MIC显著下降50%以上,为可逆抗性阶段,是控制抗性的窗口期;6~18天胞内ROS下降并恢复本底值,抗性菌显著富集,即使撤去抗生素胁迫,种群MIC基本不变,为不可逆抗性阶段。利用转录组学阐明了ROS动态变化的机制:可逆抗性阶段的ROS积累主要由于应激反应,不可逆阶段的ROS下降主要因为还原清除作用的增强。
引言:
水体和土壤等受污染环境是抗生素抗性基因(ARG)和抗生素抗性菌(ARB)的重要储存库。ARB的产生通常经历从不可遗传的耐受性和异质性抗性到可遗传抗性的过程。目前传统药敏性试验依赖于细菌生长且耗时较长。ROS的产生是细菌应对包括抗生素在内的各种胁迫的重要过程,由于高反应活性,胞内ROS无法持续累积。短期与长期抗生素胁迫下ROS的时间动态变化,以及抗生素剂量与ROS的剂量效应关系尚待深入研究。本研究依据细菌在抗生素短期胁迫下ROS动态变化特征,开发了基于ROS的抗生素抗性水平检测方法,探讨了ROS在细菌抗生素抗性发展中的指示作用,为环境细菌抗生素抗性检测提供支撑。
图文导读:
4.1 短期抗生素胁迫下细菌胞内ROS动态变化
经头孢吡肟、诺氟沙星和卡那霉素各三种浓度处理后,E. coli胞内ROS在3~4小时达到峰值,8小时左右恢复或维持在稳定水平(图1A)。低浓度胁迫(1/4 MIC)下ROS能快速恢复至正常水平,而较高浓度(≥1/2 MIC)下ROS峰值可超过100倍。抗生素胁迫下,与氧化应激、膜结构、外排泵、DNA修复等相关基因在4~8小时均出现显著上调,共同造成了ROS水平在后期下降。
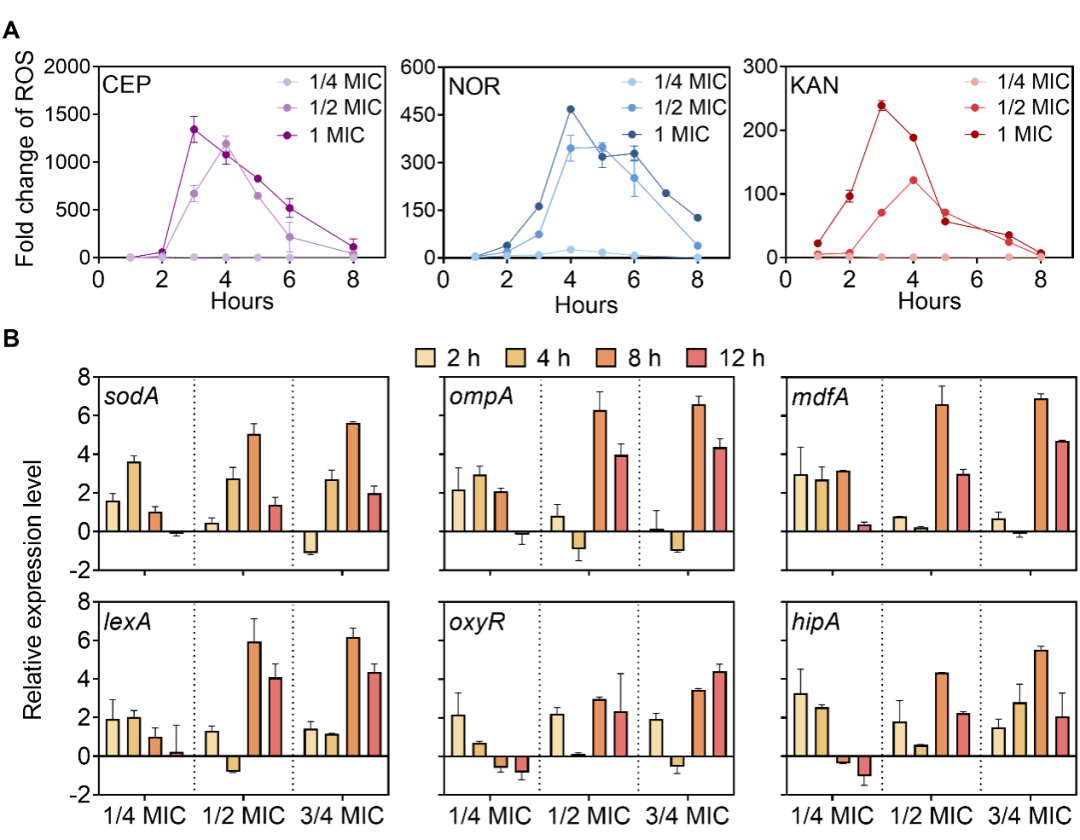
图1: E. coli在抗生素胁迫下胞内ROS时间动态变化及差异基因表达情况
4.2 抗生素浓度与胞内ROS的剂量-效应关系
由于胞内ROS通常在抗生素胁迫后3~4小时达到峰值,进一步分析了3小时的ROS(ROSt=3 h)与抗生素浓度的剂量-效应关系。抗生素浓度低于1/4 MIC时,细菌可通过基因表达调控清除ROS;浓度在1/4~1 MIC范围内,ROSt=3 h随抗生素浓度升高而增加;超过1 MIC后,由于过多细胞死亡引起ROS泄漏,ROSt=3 h下降(图2A)。对于卡那霉素抗性菌(图2B)以及从水土中分离的四种细菌(图2C),其ROSt=3 h均表现出相似的剂量-效应关系。基于此,提出ROSt=3 h峰值对应的抗生素浓度即为MIC。ROS-AST方法与微量肉汤稀释法测定的MIC值强线性相关(图2D)。该方法检测上述26种环境细菌对3种抗生素的MIC(MIC范围:0.03~128 µg/mL)具有较高的准确性,平均相对误差为7.23±13.43%。
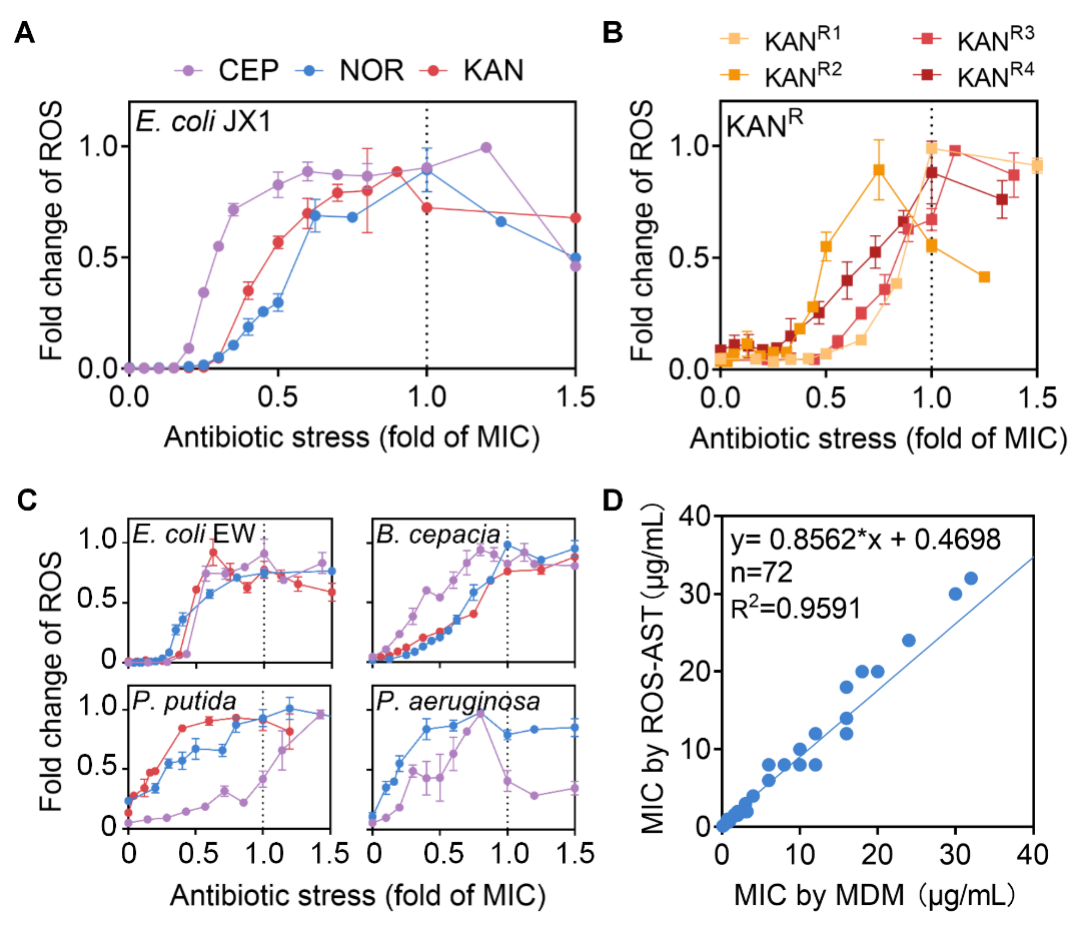
图2:不同浓度抗生素胁迫3小时后细菌胞内ROS与MIC的相关性
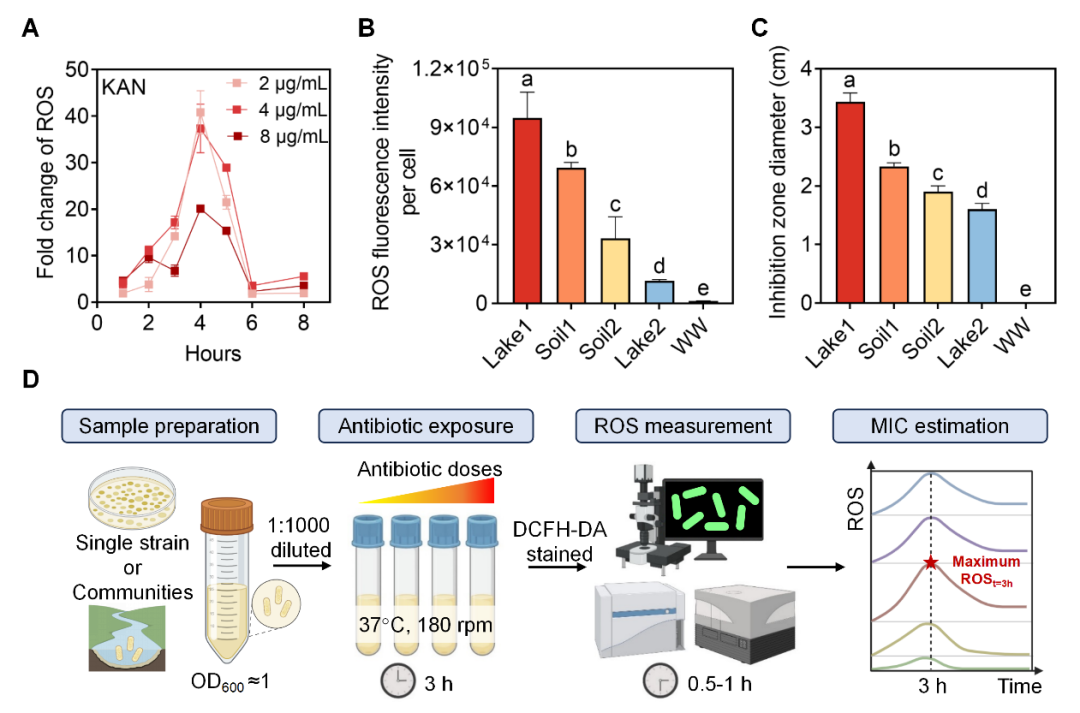
污水等环境细菌群落在抗生素胁迫后胞内ROS同样呈现先升后降的模式,在抗生素暴露后3~4小时达到峰值,6小时左右趋于稳定(图3A)。在同浓度卡那霉素胁迫下,各群落的ROSt=3 h差异显著(图3B和C),其敏感性排序与圆片扩散法结果基本一致。
ROS-AST工作流程如图3D所示。由于ROS产生受pH、温度、营养等环境条件影响,且这些条件也可能间接影响抗生素有效性,ROS-AST需在标准化条件下进行,以确保结果可比性和重复性。
4.3 胞内ROS动态变化区分抗性发展的可逆和不可逆阶段
以1 µg/mL卡那霉素连续胁迫E. coli18天,前6天ROSt=3 h显著积累随后下降, MIC和抗性菌比例显著增加(图4A和B)。第3天和第6天的种群撤去抗生素胁迫后,种群MIC降幅超过50%,而第18天的群体在撤去抗生素后MIC变化不显著,表明前6天形成的抗性是可逆的,而后转变为不可逆(图4C)。与可逆抗性阶段相比,不可逆抗性阶段细菌的生物膜形成增强、膜通透性降低、增强还原过程取代外排泵激活,同时应激反应减少(图4D和E)。
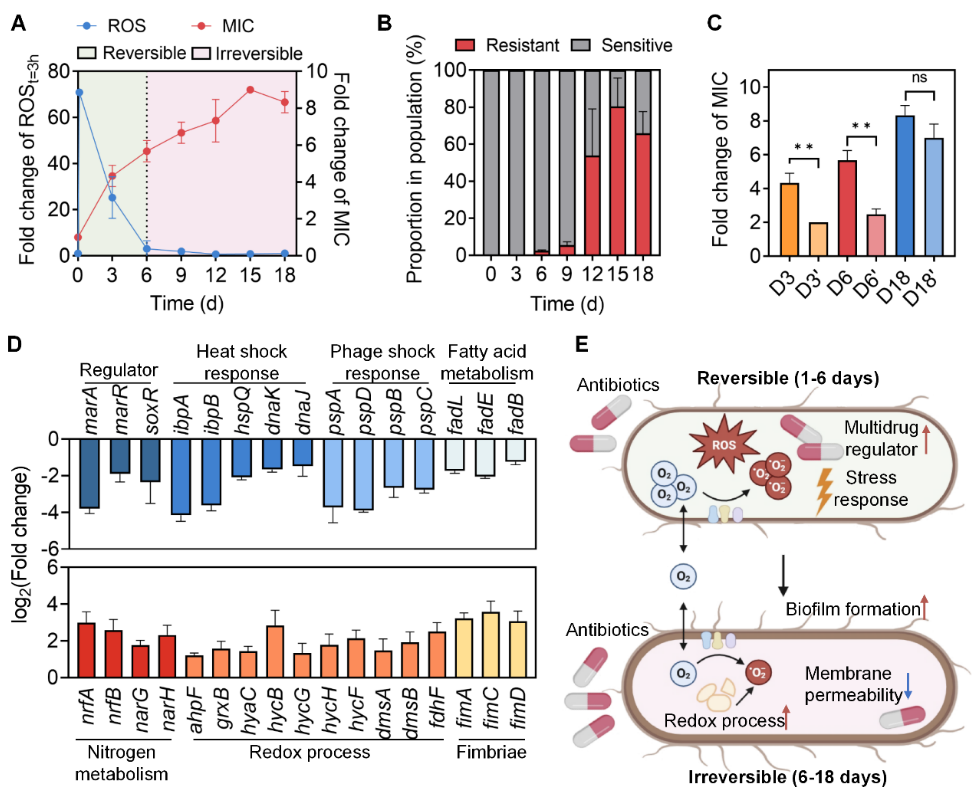
图4:E. coli在1 µg/mL卡那霉素长期胁迫下的ROS及抗性水平变化
本研究以环境分离的E. coli为模式菌株,研究了抗生素短期胁迫下ROS动态变化规律及其与抗生素抗性的剂量-效应关系,开发了可快速检测细菌及群落抗生素抗性水平的方法ROS-AST。在亚抑制浓度抗生素长期胁迫下,胞内ROS动态变化也可指示细菌抗生素抗性由可逆向不可逆的转变。该成果为环境抗性风险的快速评估与预警提供了新方法。
原文链接:https://www.sciencedirect.com/science/article/pii/S1001074225002293


